鑒于醫(yī)療器械創(chuàng)新發(fā)展迅猛和全球化發(fā)展趨勢(shì),實(shí)施醫(yī)療器械臨床試驗(yàn)前安全性評(píng)價(jià)GLP管理是大勢(shì)所趨,。國(guó)家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評(píng)中心已經(jīng)成立了醫(yī)療器械動(dòng)物實(shí)驗(yàn)研究相關(guān)指導(dǎo)原則起草制定工作組,,正在陸續(xù)發(fā)布針對(duì)具體類別的臨床前動(dòng)物實(shí)驗(yàn)研究相關(guān)指導(dǎo)原則。中國(guó)食品藥品檢定研究院醫(yī)療器械檢定所初步搭建了醫(yī)療器械臨床前動(dòng)物實(shí)驗(yàn)研究平臺(tái),。相信醫(yī)療器械動(dòng)物實(shí)驗(yàn)研究領(lǐng)域會(huì)很快建立起健全的規(guī)范管理體系,,為國(guó)內(nèi)醫(yī)療器械的創(chuàng)新發(fā)展和百姓的用械安全保駕護(hù)航。生物藥臨床前動(dòng)物實(shí)驗(yàn)公司,;江蘇有什么臨床前動(dòng)物實(shí)驗(yàn)檢測(cè)
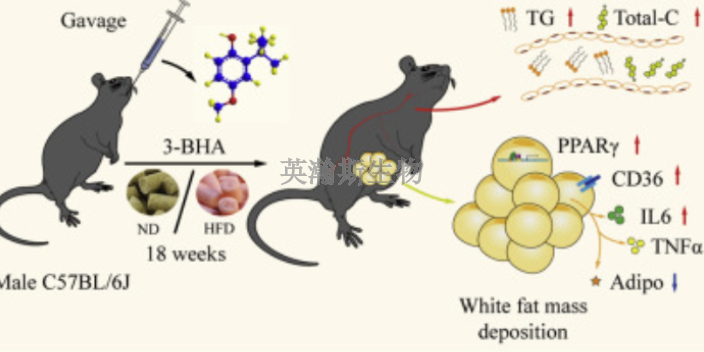
臨床前動(dòng)物實(shí)驗(yàn)?zāi)P瓦x擇的思路應(yīng)遵循以下原則:一是要很大程度地模擬預(yù)期臨床應(yīng)用的實(shí)驗(yàn)系統(tǒng),,包括動(dòng)物及其相關(guān)環(huán)境和生理特性。二是臨床前動(dòng)物實(shí)驗(yàn)研究實(shí)施的合理性,,風(fēng)險(xiǎn)分析要素應(yīng)涉及為什么選擇該動(dòng)物模型,。如果動(dòng)物模型有局限性,器械的一些相關(guān)風(fēng)險(xiǎn)比較好通過(guò)實(shí)驗(yàn)室或者尸體實(shí)驗(yàn)進(jìn)行評(píng)價(jià),,并確定其相關(guān)性。除此之外,,還應(yīng)確定實(shí)驗(yàn)系統(tǒng)的遺傳學(xué)差異(動(dòng)物和人的差異),。如實(shí)驗(yàn)系統(tǒng)和人的不同、器械的尺寸和輸送系統(tǒng)差異,、器械植入的部位和追蹤方式差異,,等等。甘肅比較好的臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)英瀚斯是專業(yè)的醫(yī)療器械臨床前動(dòng)物實(shí)驗(yàn)外包公司,。

作為**個(gè)可植入的,、第三代心室輔助裝置——磁液雙懸浮血泵“火箭心”,已經(jīng)進(jìn)入批量生產(chǎn)的臨床前動(dòng)物實(shí)驗(yàn)期,。目前進(jìn)行的動(dòng)物實(shí)驗(yàn)主要是觀察血泵的血液動(dòng)力學(xué)參數(shù),、生物相容性以及對(duì)動(dòng)物身體的影響情況。下一步將開(kāi)展生物醫(yī)學(xué)和工程學(xué)檢測(cè),。完成至少6批次的動(dòng)物實(shí)驗(yàn)后,,即可進(jìn)入臨床試用階段。慢性心力衰竭是心血管病中比較常見(jiàn)而且危害比較大的疾病之一,,目前我國(guó)有1600多萬(wàn)心衰患者,。目前對(duì)于心衰的,一般采取藥物,、外科手術(shù),、機(jī)械輔助循環(huán)及心臟移植,。
臨床前動(dòng)物實(shí)驗(yàn)的目的主要是通過(guò)相關(guān)動(dòng)物模型來(lái)考察產(chǎn)品的安全性和有效性,以及臨床相關(guān)參數(shù)的確定,,預(yù)測(cè)其在人群中使用時(shí)可能出現(xiàn)的不良事件,,降低臨床試驗(yàn)受試者和臨床使用者承擔(dān)的風(fēng)險(xiǎn),并為臨床試驗(yàn)方案的制定提供依據(jù),。動(dòng)物實(shí)驗(yàn)研究作為初步驗(yàn)證醫(yī)療器械安全性及有效性的重要手段,,動(dòng)物實(shí)驗(yàn)的質(zhì)量管理對(duì)保證動(dòng)物實(shí)驗(yàn)研究數(shù)據(jù)的真實(shí)、可靠,、準(zhǔn)確,、科學(xué)和完整至關(guān)重要。因此,,研究機(jī)構(gòu)需要加強(qiáng)對(duì)臨床前動(dòng)物實(shí)驗(yàn)的質(zhì)量管理,,監(jiān)管部門(mén)也將不斷加強(qiáng)對(duì)該領(lǐng)域的規(guī)范要求并加強(qiáng)科學(xué)監(jiān)管。生物藥臨床前動(dòng)物實(shí)驗(yàn)是什么,?
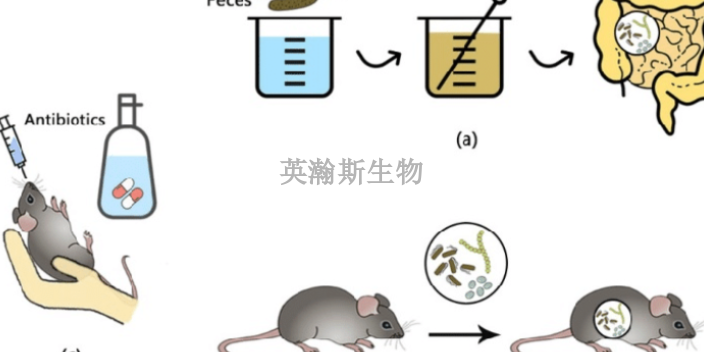
臨床前動(dòng)物實(shí)驗(yàn)研究監(jiān)測(cè)②中期觀察:在動(dòng)物從初始手術(shù)過(guò)程中恢復(fù),,監(jiān)測(cè)器械相關(guān)風(fēng)險(xiǎn)期間,建議每天至少在喂食時(shí)間監(jiān)測(cè)兩次,,以便在活動(dòng)時(shí)觀察它們,。同時(shí),建議咨詢獸醫(yī)并制定體重監(jiān)測(cè)計(jì)劃,。應(yīng)考慮將體重評(píng)分作為定期觀察動(dòng)物的輔助手段,。如果研究涉及收集臨床生化檢測(cè)數(shù)據(jù)或更先進(jìn)的診斷,建議制定標(biāo)準(zhǔn)操作規(guī)程以便在需要時(shí)指定一種不械的化學(xué)干預(yù)方法,。③終期研究期:建議實(shí)驗(yàn)方案應(yīng)包括終期研究的細(xì)節(jié),,并包括檢查、采集和組織處理的所有方法,。具體方案應(yīng)包括終點(diǎn)檢驗(yàn)的方法,、完成放射線分析和成像分析的陳述(如果適用)、確定**終體重和機(jī)體評(píng)分的方法,。④尸體解剖和評(píng)估:不良事件可能會(huì)出現(xiàn)在臨床或亞臨床期,。因此,建議在研究中納入的系統(tǒng)性尸檢,,包括組織收集和保存,,以進(jìn)行組織病理學(xué)檢查。所得信息可協(xié)助確定不良事件與器械的相關(guān)性,?;瘜W(xué)藥臨床前動(dòng)物實(shí)驗(yàn)機(jī)構(gòu);陜西高質(zhì)量臨床前動(dòng)物實(shí)驗(yàn)是什么
生物藥臨床前動(dòng)物實(shí)驗(yàn)指導(dǎo)原則,;江蘇有什么臨床前動(dòng)物實(shí)驗(yàn)檢測(cè)
當(dāng)臨床前動(dòng)物實(shí)驗(yàn)結(jié)果顯示化合物具有足夠的安全性并準(zhǔn)備進(jìn)入人體試驗(yàn)時(shí)主辦者需要向FDA申請(qǐng)新藥臨床試驗(yàn)investigationalNewDrugApplication,ND申請(qǐng)),。按照美國(guó)食品,、藥品和化妝品法案(Food,DrugandCosmeticAct),此時(shí)的化合物已經(jīng)成為研究藥物,將受到官方的監(jiān)管。FDA收到藥物申報(bào)主辦者遞交的IND時(shí),藥物申報(bào)主辦者,即負(fù)責(zé)藥物上市的公司硏究機(jī)構(gòu)和其他組織,必須向FDA提供其對(duì)實(shí)驗(yàn)動(dòng)物所進(jìn)行臨床前試驗(yàn)的結(jié)果,以及進(jìn)行人體試驗(yàn)的具體計(jì)劃,。在這個(gè)階段,FDA必須判斷藥物是否安全,是否達(dá)到實(shí)施人體試驗(yàn)的標(biāo)準(zhǔn),。江蘇有什么臨床前動(dòng)物實(shí)驗(yàn)檢測(cè)



